Ch 2.2 La classification
périodique des éléments
Ce
TP cours se traite en 2 séances
1.La
première classification périodique des éléments
Avant
1700, seuls 12 corps
simples avaient été isolés ; en 1850, on en connaissait
61 !
L'étude
des propriétés des corps simples connus permit la mise en évidence
d'analogies
: ainsi, en 1808, H. Davy montra que le calcium, le strontium et le
baryum
avaient des propriétés voisines.
La
définition d'un système de
masses
atomiques (masse des atomes) vers 1860 offrit un critère quantitatif de
classement des corps simples.

En
1869, un professeur russe, Dimitri Mendeleïev classe les éléments par
ordre de
masse atomique croissante et rassemble dans une même colonne les
éléments
possédant des propriétés voisines.
1.
A
l’époque de Mendeleïev,
parlait-on
d’atomes ?
oui,
on en parlait à nouveau depuis le
début du 19ème siècle )
connaissait-on
les électrons ?
non,
ils n’ont été
découverts qu’en 1895
Le
numéro atomique ?
non
2.Travail
à effectuer
Sortir
les cartes
des
éléments de l'enveloppe et constituer 8
groupes de plusieurs éléments ayant les mêmes
propriétésen utilisant les propriétés des
corps simples et les formules des corps composés.
3. Question
Quel
fut le premier critère
quantitatif permettant une classification des
éléments ?
masse
atomique.
4.
Mendeleïev
classe les éléments en plaçant
- sur
une même ligne les éléments par ordre de masse
atomique croissante.
- sur
une même colonne les éléments qui ont les mêmes propriétés
5.Application
Essayer de retrouver une
partie de
la classification
périodique en utilisant la même méthode que Mendeleïev. Pour cela,
placer les
cartes de
façon à respecter les deux critères de
Mendeleïev, puis remplir les cases du tableau
1 par le symbole et le nom de chaque élément. ( il
peut y avoir des
cases vides ! )
Tableau 1
| H |
|
|
|
|
|
|
He |
| Li |
Be |
B |
C |
N |
O |
F |
Ne |
| Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
| K |
|
|
|
|
|
|
|
Remarque :
en réalité,
Mendeleïev avait inversé les lignes et les colonnes…. Voir livre doc 1
p 248
Il
avait laissé des cases vides,
pour des éléments encore inconnus…
( voir diaporama
)
2. Répartition
des électrons d’un atome
2.1 Le nuage
électronique
2.1.1 Les
couches
électroniques
Tous
les électrons sont identiques
Mais
ils ne sont pas tous liés de la même façon au noyau.
Exemple :
L’atome
de sodium
possède 2
électrons très liés au noyau
8
électrons liés au noyau
1
électron très peu lié au noyau
Les
électrons sont répartis en différentes couches,
que l’on
représente par
des
numéros ( 1, 2, 3…) ou notées K,
L, M … de plus en plus éloignées du
noyau.
2.1.2 Règles
de
remplissage de Pauli ( 1900 - 1958 )
Les couches électroniques
contiennent un nombre limité d’électrons
La
couche K contient …2
.électrons
La
couche L contient …8…..électrons
La
couche M contient …8….électrons
Des
électrons remplissent d’abord la couche K,
puis
quand elle est pleine,
la couche L,
etc.
La couche la plus éloignée
du noyau
est appelée couche
externe : elle contient les électrons les moins
liés au noyau.
2.1.3.Application
Remplir le tableau suivant
en
notant la structure
électronique ( ou
modèle électronique )
sous la forme :
(K) x(
L )y ( M )z x,
y, et z étant les nombres d'électrons dans les différentes couches d'un
atome
dans son état fondamental.
Tableau 2
| Elément |
hydrogène
|
hélium
|
lithium |
Béryllium |
Bore |
carbone |
azote |
| Symbole
(Z) |
1H |
2He |
3Li |
4Be |
5B |
6C |
7N |
| Structure
électronique |
(K)1 |
(K)2 |
(K)2(L)1 |
(K)2(L)2 |
(K)2(L)3 |
(K)2(L)4 |
(K)2(L)5 |
|
|
|
|
|
|
|
|
| Elément |
oxygène |
fluor |
Néon |
sodium |
magnésium |
aluminium |
silicium |
| Symbole
(Z) |
8O |
9F |
10Ne |
11Na |
12Mg |
13Al |
14Si |
| Structure
électronique |
(K)2(L)6
|
(K)2(L)7 |
(K)2(L)8 |
(K)2(L)8(M)1 |
(K)2(L)8(M)2 |
(K)2(L)8(M)3 |
(K)2(L)8(M)4 |
|
|
|
|
|
|
|
|
| Elément |
Phosphore |
soufre |
chlore |
Argon |
|
| Symbole
(Z) |
15P |
16S
|
17Cl
|
18Ar |
|
| Structure
électronique |
(K)2(L)8(M)5 |
(K)2(L)8(M)6 |
(K)2(L)8(M)7
|
(K)2(L)8(M)8
|
|
2.2 Classification
périodique actuelle
A
partir des tableaux 1 et 2,
compléter le tableau 3 en vous inspirant de l’exemple donné, et, en
indiquant uniquement
la structure de la couche externe.
| H |
|
He |
| (K)1 |
(K)2 |
| Li |
Be |
B |
C |
N |
O |
F |
Ne |
| (L)1 |
(L)2 |
(L)3 |
(L)4 |
(L)5 |
(L)6 |
(L)7 |
(L)8 |
| Na |
Mg |
Al |
Si |
P |
S |
Cl |
Ar |
| (M)1 |
(M)2 |
(M)3
|
(M)4 |
(M)5 |
(M)6 |
(M)7 |
(M)8 |
Conclusions:
Dans la classification périodique des éléments actuelle,
les éléments sont
classés par numéro atomique (Z) croissant.
Les éléments d'une
même colonne ont le même nombre d' électrons sur la couche externe
Chaque ligne du
tableau correspond au remplissage d'une nouvelle couche.
3. COMPORTEMENT CHIMIQUE D'UNE FAMILLE D'ELEMENTS
3.1 Les alcalino-terreux
Les éléments de la 2ème colonne de la
classification périodique forment la famille des alcalino-terreux :
béryllium ( Be) , magnésium ( Mg), calcium (Ca).
3.1.1 Réaction du calcium avec l’eau acidifiée
Dans un tube à essais, introduire un morceau de calcium, puis environ 3
mL d’eau acidifiée. Boucher
Observations
Le calcium est un métal mou, gris.
 Vive effervescence
Vive effervescence

Caractérisation du gaz
 Le gaz formé est du dihydrogène H2
Le gaz formé est du dihydrogène H2
Réaction chimique
Les ions H+ de
l'acide se sont transformés en dihydrogène ; les atomes de
calcium Ca se sont transformés en ions Ca2+(
incolores) en perdant 2 électrons.
3.1.2 Réaction du magnésium avec l’eau acidifiée
Dans un tube à essais, introduire un morceau de magnésium, puis environ
3 mL d’eau acidifiée. Boucher
Observations
Le magnésium est un métal mou, gris.
 Vive
effervescence
Vive
effervescence 
Caractérisation du gaz
 Le gaz formé est du dihydrogène H2
Le gaz formé est du dihydrogène H2
Réaction chimique
Les ions H+ de
l'acide se sont transformés en dihydrogène ; les atomes
de magnésium Mg se sont transformés en ions Mg2+(
incolores) en perdant 2 électrons.
3.1.3 Conclusion
Ces 2 réactions
faites par Mg et Ca se ressemblent beaucoup.
3.2 Réactions chimiques avec les halogènes
Les éléments de l'avant - dernière colonne de la classification
périodique forment la famille des halogènes :
F ( fluor ) ; Cl ( chlore ) ; Br ( brome ) ; I ( iode ) ; At ( astate ).
3.2.1 Présentation des dihalogènes
Les dihalogènes : Cl2 : dichlore
, Br2 : dibrome
et I2 : diiode
sont des corps purs.
Ce sont des espèces chimiques très toxiques donc dangereuses.
A température ambiante,
 Cl2 est un gaz de couleur
verte
,
Cl2 est un gaz de couleur
verte
,
Br2 est
un liquide de
couleur rouge
et I2 est un solide gris
 (dont la vapeur est violette).
(dont la vapeur est violette).
3.2.2 Les ions halogènures
Les halogènures de potassium ( KCl, KBr et KI ) sont des solides non
toxiques, solubles dans l'eau et donnant des solutions incolores.
Réaction avec les ions argent : Ag +
|
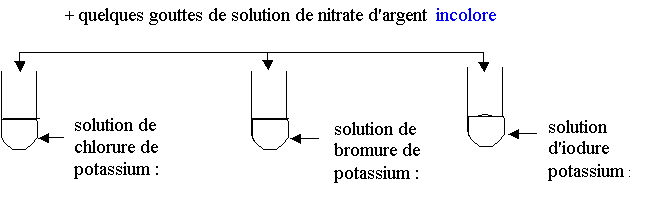 |
| Observation |
Formation
instantanée d'un précipité blanc de
chlorure d'argent |
Formation
instantanée d'un précipité blanc de bromure d'argent |
Formation
instantanée d'un précipité blanc de iodure d'argent |
| Réaction |
Ag++Cl-→
AgCl(s) |
Ag++Br-→
AgBr(s) |
Ag++I-→
AgI(s) |
Ces 3 réactions se
ressemblent beaucoup.
3.3 Conclusion
Par ces 2 séries
d'exemples ( alcalino-terreux et halogènes) , on a illustré le fait que
des éléments qui sont dans la même
colonne de la classification périodique font des réactions chimiques semblables.


 Vive effervescence
Vive effervescence

 Le gaz formé est du dihydrogène H2
Le gaz formé est du dihydrogène H2 Vive
effervescence
Vive
effervescence  Cl2 est un
Cl2 est un 
 (dont la vapeur est violette).
(dont la vapeur est violette).